Forståelse af kliniske forsøg
Kliniske forsøg er medicinske undersøgelser, der ser på potentielle nye lægemidler, procedurer og andre behandlinger hos mennesker, der er ramt af sygdomme som kræft. I hele denne proces forsøger læger at afgøre, om disse potentielle nye behandlinger er sikre og effektive. For det meste undersøges det også, om behandlingerne vil bidrage til at forbedre patienternes livskvalitet. Kræftpatienters deltagelse i kliniske forsøg bidrager til medicinsk og videnskabelig viden om kræft og kan forbedre nuværende og fremtidig behandling.
Hvad er kliniske forsøg?
Kliniske forsøg er en lang proces, der starter i laboratoriet. Før nogen ny behandling gives til mennesker, bruger forskere ofte mange år på at forstå dens virkninger gennem test. I disse tests forsøger forskere at lære så meget som muligt om, hvordan behandlingen virker i celler og dyr.
Forskere planlægger hvert klinisk forsøg for at teste specifikke spørgsmål. De kan være på udkig efter at finde behandlinger som:
Før at en behandling kan tages i brug, skal det nye kræftlægemiddel være effektiv og relativt sikkert at tage. Derfor følger forskere omhyggeligt patienternes oplevelser i de kliniske forsøg. På denne måde kan de identificere eventuelle sikkerhedsproblemer eller bivirkninger.
Kliniske forsøg kan finde sted på hospitaler, universiteter, og eller i lægepraksis. Et forsøg kan vare uger eller år, afhængigt af hvad der undersøges, og hvad målene er. Deltagerne får at vide, hvor længe forsøget vil vare, før de tilmelder sig. Efterhånden som telemedicinsk (digital) teknologi er blevet mere tilgængelig og forbedret kan visse patienter nu følges i deres eget miljø under et kliniske kræftforsøg
Grundlæggende om deltagelse i kliniske forsøg
Før nogen kan deltage i et klinisk forsøg, skal de opfylde visse krav. Faktorer, der er nødvendige for, at en person kan deltage, kaldes "inklusionskriterier", mens de, der forhindrer nogen i at deltage, kaldes "eksklusionskriterier". For eksempel kan et forsøgs inklusionskriterier kræve, at enhver deltagende patient diagnosticeres med myelomatose og er inden for en bestemt aldersgruppe. Alternativt tillader et forsøgs eksklusionskriterier muligvis ikke nogen patienter, der er gravide. Kravene til hvert klinisk forsøg fører tilbage til de spørgsmål, som det kliniske forsøg forsøger at besvare.
Beslutningen om at deltage skal være helt frivillig. Enhver, der beslutter at deltage i et forsøg, vil blive bedt om at give skriftlig tilladelse, kendt som "informeret samtykke". Processen, der fører til informeret samtykke, hjælper med at uddanne en potentiel deltager om alle aspekter og potentielle risici ved det kliniske forsøg, de er ved at indgå i. Dette er for, at de kan træffe den rigtige beslutning for dem.
Flere organisationer rundt om i verden, såsom Det Europæiske Lægemiddelagentur (EMA) og den danske lægemiddelstyrelse beskytter patienter i kliniske forsøg ved at håndhæve regler om, hvordan behandlinger gives og risici overvåges.
Faser af den kliniske forsøgsproces
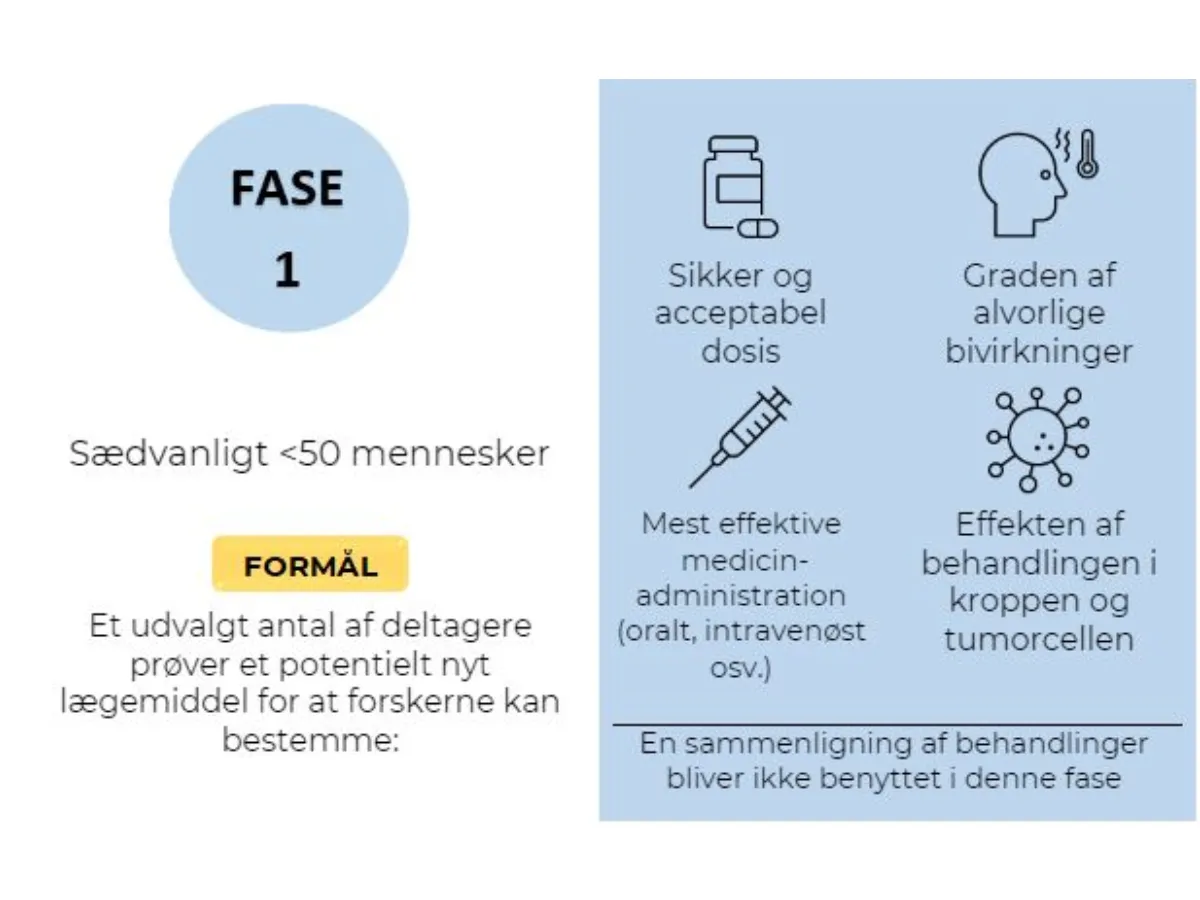
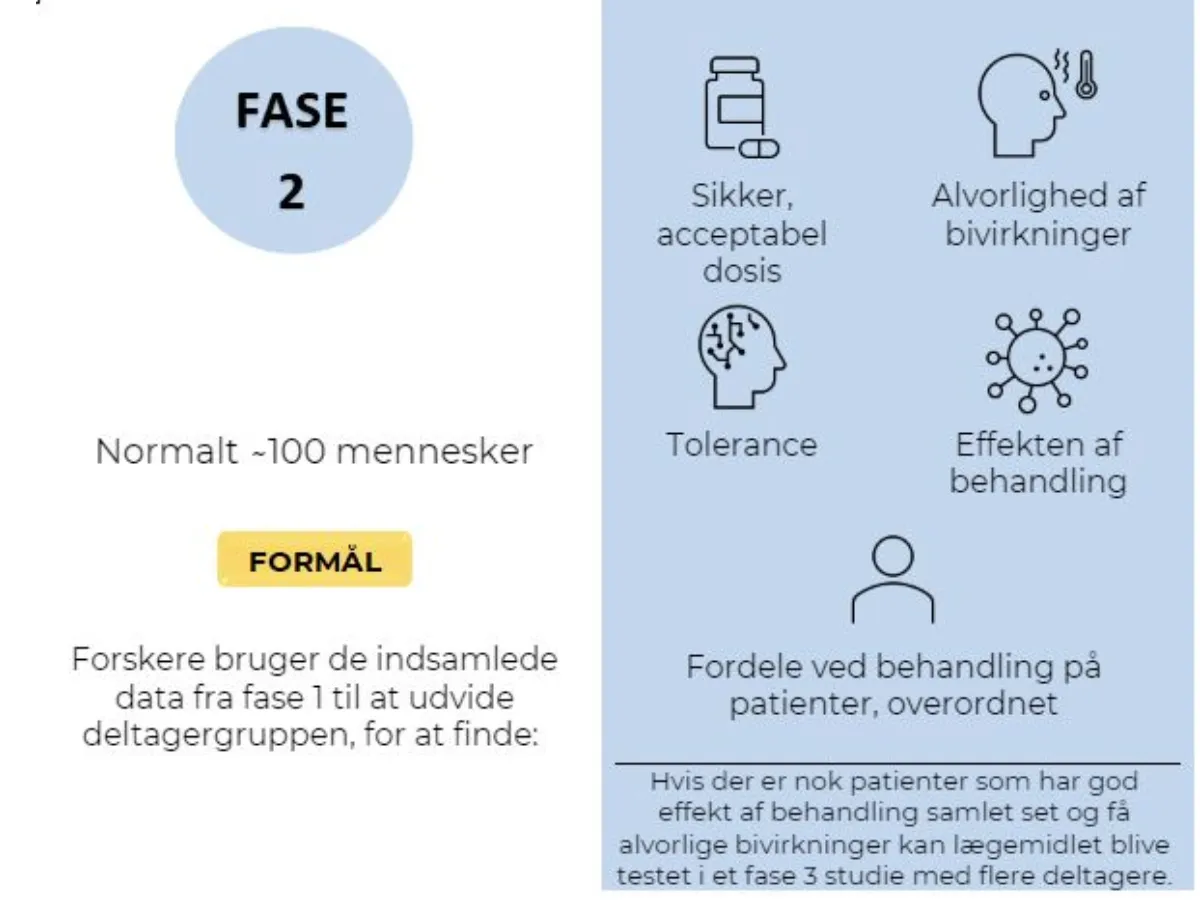
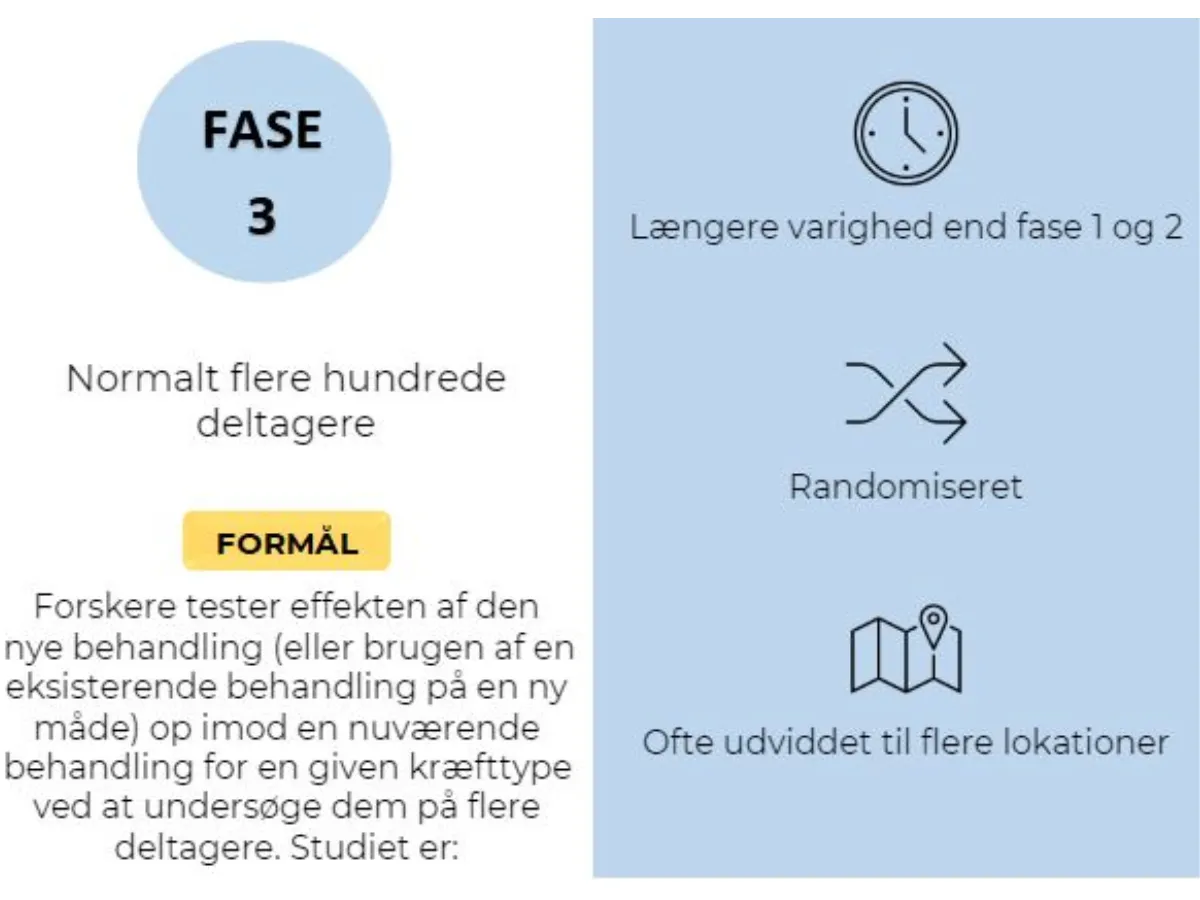
Ved test af potentiel ny behandling er der involveret en række kliniske trin, kaldet faser. Hver fase giver visse oplysninger om behandlingen. Hvis en potentiel ny behandling er vellykket i en fase, kan den gå videre til yderligere test i den næste fase. At kende fasen for det kliniske forsøg er vigtigt for deltagerne, fordi det giver indsigt i, hvor meget der i forvejen kendes til den undersøgte behandling, og hvilke fordele og risici der kan være involveret i at deltage.
.
Randomiseret refererer til, når undersøgelsesdeltagere tilfældigt tildeles enten den nye behandling eller den behandling, læger i øjeblikket bruger. De grupper af deltagere, der tager de forskellige behandlinger, udgør de forskellige "arme" i undersøgelsen.
Nogle gange kender hverken deltager i et fase 3-forsøg, eller dem der kører det, til, hvilken behandling hver deltager får. Denne opsætning er kendt som en "dobbeltblindet" undersøgelse. Som med tidligere faser overvåges deltagere i kliniske fase 3-forsøg nøje for bivirkninger, og behandlingen stoppes, hvis de er skadelige.
Da det er frivilligt at deltage i et klinisk forsøg, kan deltagerne vælge at forlade forsøget når som helst, for eksempel på baggrund af bivirkninger.
Hvordan måles succes i kliniske forsøg?
Målene for kliniske forsøg kaldes endepunkter og er de resultater, der viser, om et lægemiddel eller en behandling virker på de patienter, der tager behandlingen. Endepunkter kan for eksempel være, hvor længe deltagerne overlever, om deres tumor skrumper, hvor længe deres kræft kontrolleres eller deres livskvalitet.
Lægemiddelagenturerne hjælper med at give forskere information om de bedste slutpunkter til brug i deres forsøg.
Her er et par almindelige målepunkter i kliniske forsøg:
Kliniske forsøg har haft en enorm indflydelse på at forbedre kræftbehandlingen og give viden til det videnskabelige samfund. Som et resultat lever folk i dag længere end nogensinde med en kræftdiagnose. Ved at deltage i kliniske forsøg får mennesker, der lever med kræft, adgang til potentielle fremskridt inden for kræftpleje og hjælper forskere med at opdage nye, mere effektive terapier. De fleste forsøg indebærer en form for potentiel risiko for deltageren, så stil spørgsmål om forskningen, risiciene, fortrolighed og andre bekymringer der vil hjælpe dig med at få de oplysninger, du har brug for til at beslutte, om deltagelse er noget for dig.
Informationen som gives her er af generel karakter og kan ikke erstatte rådgivning af egen læge eller andet kvalificeret sundhedspersonale.
PP-UNP-DNK-0357